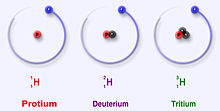
O hidrogênio tem três isótopos principais: protium (1H), deutério (2H) e tritium (3H). Estes isótopos se formam naturalmente na natureza. O protium e o deutério são estáveis. O trítio é radioativo e tem uma meia-vida de cerca de 12 anos. Os cientistas criaram outros quatro isótopos de hidrogênio (4H a 7H), mas estes isótopos são muito instáveis e não existem naturalmente.
Os principais isótopos de hidrogênio são únicos porque são os únicos isótopos que têm um nome. Estes nomes ainda estão em uso hoje. Deutério e trítio às vezes recebem seus próprios símbolos, D e T. Entretanto, a União Internacional de Química Pura e Aplicada não gosta muito desses nomes, mesmo que sejam usados com freqüência. Existem outros isótopos que tiveram seus próprios nomes quando os cientistas estudaram a radioatividade. Mas, seus nomes não são mais usados hoje em dia.