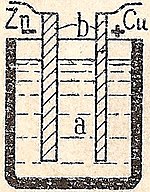
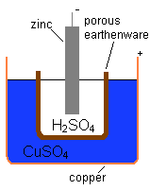
Uma célula eletroquímica que causa um fluxo externo de corrente elétrica pode ser criada usando quaisquer dois metais diferentes, uma vez que os metais diferem em sua tendência a perder elétrons. O zinco perde elétrons mais prontamente do que o cobre, portanto, a colocação de zinco e cobre metálico em soluções de seus sais pode causar o fluxo de elétrons através de um fio externo que leva do zinco ao cobre. Como um átomo de zinco fornece os elétrons, ele se torna um íon positivo e vai para uma solução aquosa, diminuindo a massa do eletrodo de zinco. No lado do cobre, os dois elétrons recebidos permitem que ele converta um íon de cobre da solução em um átomo de cobre sem carga que se deposita no eletrodo de cobre, aumentando sua massa. As duas reações são tipicamente escritas
Zn(s) --> Zn2+(aq) + 2e-
Cu2+(aq) + 2e- --> Cu(s)
As letras entre parênteses são apenas lembretes de que o zinco vai de um sólido (s) para uma solução de água (aq) e vice versa para o cobre. É típico na linguagem da eletroquímica referir-se a estes dois processos como "semi-reações" que ocorrem nos dois eletrodos.
| Zn(s) -> Zn2+(aq) + 2e- | | O zinco "semi-reação" é classificado como oxidação, uma vez que perde elétrons. O terminal no qual ocorre a oxidação é chamado de "ânodo". Para uma bateria, este é o terminal negativo. | |
| A "semi-reação" de cobre é classificada como redução, uma vez que ganha elétrons. O terminal no qual ocorre a redução é chamado de "cátodo". Para uma bateria, este é o terminal positivo. | | Cu2+(aq) + 2e- -> Cu(s) |
Para que a célula voltaica continue a produzir uma corrente elétrica externa, deve haver um movimento dos íons sulfato em solução da direita para a esquerda para equilibrar o fluxo de elétrons no circuito externo. Os íons metálicos em si devem ser impedidos de se mover entre os eletrodos, portanto, algum tipo de membrana porosa ou outro mecanismo deve prever o movimento seletivo dos íons negativos no eletrólito da direita para a esquerda.
A energia é necessária para forçar os elétrons a se moverem do zinco para o eletrodo de cobre, e a quantidade de energia por unidade de carga disponível da célula de voltagem é chamada de força eletromotriz (emf) da célula. A energia por unidade de carga é expressa em volts (1 volt = 1 joule/coulomb).
Claramente, para obter energia da célula, você deve obter mais energia liberada da oxidação do zinco do que a necessária para reduzir o cobre. A célula pode produzir uma quantidade finita de energia deste processo, sendo o processo limitado pela quantidade de material disponível no eletrólito ou nos eletrodos metálicos. Por exemplo, se houvesse uma toupeira dos íons sulfato SO42- no lado do cobre, então o processo é limitado à transferência de dois moles de elétrons através do circuito externo. A quantidade de carga elétrica contida em uma toupeira de elétrons é chamada constante de Faraday, e é igual ao número de vezes que a carga de elétrons da Avogadro:
Constante de Faraday = F = NAe = 6.022 x 1023 x 1.602 x 10-19 = 96.485 Coulombs/mole
O rendimento energético de uma célula voltaica é dado pela voltagem da célula vezes o número de moles de elétrons transferidos vezes a constante de Faraday.
Saída de energia elétrica = nFEcell
A célula emf Ecell pode ser prevista a partir dos potenciais de eletrodos padrão para os dois metais. Para a célula de zinco/cobre sob as condições padrão, o potencial calculado da célula é de 1,1 volts.