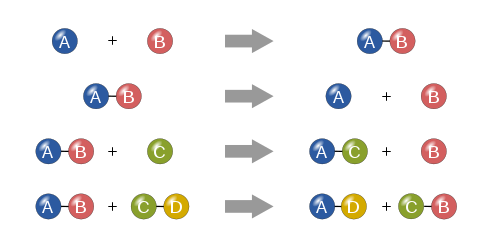
Síntese
Em uma reação de síntese, duas ou mais substâncias simples se combinam para formar uma substância mais complexa.
A + B ⟶ A B {\displaystyle A+B\longrightarrow AB} 
"Dois ou mais reagentes dando um produto" é outra forma de identificar uma reação de síntese. Um exemplo de uma reação de síntese é a combinação de ferro e enxofre para formar o sulfeto de ferro(II):
8 F e + S 8 ⟶ 8 F e S {\i1}displaystyle 8Fe+S_{\i1}longrightarrow 8FeS 
Outro exemplo é o gás hidrogênio simples combinado com gás oxigênio simples para produzir uma substância mais complexa, como a água.
Decomposição
Uma reação de decomposição é quando uma substância mais complexa se decompõe em suas partes mais simples. É, portanto, o oposto de uma reação de síntese, e pode ser escrita como:
A B ⟶ A + B {\displaystyle AB\longrightarrow A+B} 
Um exemplo de uma reação de decomposição é a eletrólise da água para produzir oxigênio e hidrogênio gasoso:
2 H 2 O ⟶ 2 H 2 + O 2 {\i1}O 2H_{\i1}O 2H_{\i1}+O_O_{\i}}longrightarrow 2H_{\i} 
Substituição única
Em uma única reação de substituição, um único elemento não combinado substitui outro em um composto; em outras palavras, um elemento comercializa lugares com outro elemento em um composto Essas reações vêm na forma geral de
A + B C ⟶ A C + B {\displaystyle A+BC\longrightarrow AC+B} 
Um exemplo de uma única reação de deslocamento é quando o magnésio substitui o hidrogênio na água para fazer hidróxido de magnésio e hidrogênio gasoso:
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 Mg+2H_{2}O{2}O{2}longrightarrow Mg(OH)_{2}+H_{2}} 
Substituição dupla
Em uma dupla reação de substituição, os ânions e cátions de dois compostos trocam de lugar e formam dois compostos totalmente diferentes. Estas reações estão na forma geral:
A B + C D ⟶ A D + C B {\displaystyle AB+CD\longrightarrow AD+CB} 
Por exemplo, quando o cloreto de bário (BaCl2) e o sulfato de magnésio (MgSO4) reagem, o SO42- anion comuta com o anion 2Cl-, dando aos compostos BaSO4 e MgCl2.
Outro exemplo de reação de deslocamento duplo é a reação de nitrato de chumbo(II) com iodeto de potássio para formar iodeto de chumbo(II) e nitrato de potássio:
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {\i1}displaystyle Pb(NO_{3})_{2}+2KI}longrightarrow PbI_{2}+2KNO_{3}}