Os elétrons têm a menor carga elétrica. Esta carga elétrica é igual à carga de um próton, mas tem o sinal oposto. Por esta razão, os elétrons são atraídos pelos prótons dos núcleos atômicos e geralmente formam átomos. Um elétron tem uma massa de cerca de 1/1836 vezes um protão.
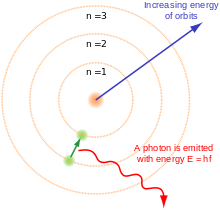
Uma maneira de pensar sobre a localização dos elétrons em um átomo é imaginar que eles orbitam a distâncias fixas do núcleo. Desta forma, os elétrons em um átomo existem em uma série de conchas de elétrons que circundam o núcleo central. A cada concha de elétron é dado um número 1, 2, 3, e assim por diante, a partir daquele mais próximo do núcleo (a concha mais interna). Cada concha pode conter até um certo número máximo de elétrons. A distribuição de elétrons nas diversas conchas é chamada de disposição eletrônica (ou forma ou forma eletrônica). A disposição eletrônica pode ser mostrada pela numeração ou por um diagrama eletrônico. (Uma maneira diferente de pensar sobre a localização dos elétrons é usar a mecânica quântica para calcular suas orbitais atômicas).
O elétron é um dos tipos de partículas subatômicas chamadas leptões. O elétron tem uma carga elétrica negativa. O elétron tem outra propriedade, chamada spin. Seu valor de spin é 1/2, o que o torna um férmion.
Enquanto a maioria dos elétrons são encontrados em átomos, outros se movem independentemente na matéria, ou juntos como raios catódicos em um vácuo. Em alguns supercondutores, os elétrons se movimentam em pares. Quando os elétrons fluem, este fluxo é chamado de eletricidade, ou uma corrente elétrica.
Um objeto pode ser descrito como 'negativamente carregado' se houver mais elétrons que prótons em um objeto, ou 'positivamente carregado' quando houver mais prótons que elétrons. Os elétrons podem se mover de um objeto para outro quando tocados. Eles podem ser atraídos para outro objeto com carga oposta, ou repelidos quando ambos têm a mesma carga. Quando um objeto é 'aterrado', os elétrons do objeto carregado vão para o solo, tornando o objeto neutro. Isto é o que os pára-raios (pára-raios) fazem.
Reações químicas
Os elétrons em suas conchas ao redor de um átomo são a base das reações químicas. As conchas externas completas, com o máximo de elétrons, são menos reativas. As conchas externas com menos do que o máximo de elétrons são reativas. O número de elétrons nos átomos é a base da tabela periódica de produtos químicos.
Medição
A carga elétrica pode ser medida diretamente com um dispositivo chamado eletromedidor. A corrente elétrica pode ser medida diretamente com um galvanômetro. A medida emitida por um galvanômetro é diferente da medida emitida por um eletrometro. Hoje, os instrumentos de laboratório são capazes de conter e observar elétrons individuais.
"Ver" um elétron
Em condições de laboratório, as interações de elétrons individuais podem ser observadas por meio de detectores de partículas, que permitem a medição de propriedades específicas, tais como energia, rotação e carga. Em um caso, uma armadilha de caneta foi usada para conter um único elétron durante 10 meses. O momento magnético do elétron foi medido com precisão de onze dígitos, o que, em 1980, era uma precisão maior do que para qualquer outra constante física.
As primeiras imagens em vídeo da distribuição de energia de um elétron foram capturadas por uma equipe da Universidade de Lund, na Suécia, em fevereiro de 2008. Os cientistas usaram flashes de luz extremamente curtos, chamados pulsos de atosegundo, que permitiram que o movimento de um elétron fosse observado pela primeira vez. A distribuição dos elétrons em materiais sólidos também pode ser visualizada.
Anti-partícula
A antipartícula do elétron é chamada de positron. Este é idêntico ao elétron, mas carrega cargas elétricas e outras cargas do sinal oposto. Quando um elétron colide com um positron, ele pode se espalhar ou ser totalmente aniquilado, produzindo um par (ou mais) de fótons de raios gama.