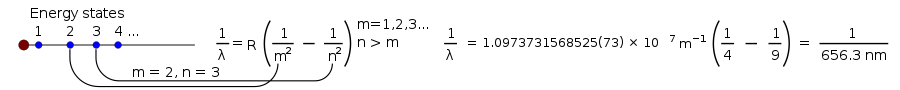As fórmulas e idéias da mecânica quântica foram feitas para explicar a luz que vem do hidrogênio incandescente. A teoria quântica do átomo também teve que explicar porque o elétron permanece em sua órbita, o que outras idéias não foram capazes de explicar. Seguiu-se das idéias mais antigas que o elétron teria que cair para o centro do átomo porque começa a ser mantido em órbita por sua própria energia, mas rapidamente perderia sua energia ao girar em sua órbita. (Isto porque os elétrons e outras partículas carregadas eram conhecidos por emitir luz e perder energia quando mudavam de velocidade ou giravam).
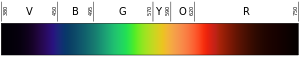
As lâmpadas de hidrogênio funcionam como luzes de néon, mas as luzes de néon têm seu próprio grupo único de cores (e freqüências) de luz. Os cientistas aprenderam que podiam identificar todos os elementos pelas cores de luz que produzem. Eles simplesmente não conseguiam descobrir como as freqüências eram determinadas.
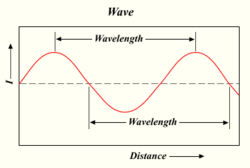
Então, um matemático suíço chamado Johann Balmer descobriu uma equação que dizia o que seria λ (lambda, para comprimento de onda):
λ = B ( n 2 n 2 - 4 ) n = 3 , 4 , 5 , 6 {\i1}displaystyle {\i1}lambda = B esquerda(n^{\i}{n^2}{n^{\i}-4}}{n^2 n^2 - 4}qquadad n=3,4,5,6} 
onde B é um número que Balmer determinou ser igual a 364,56 nm.
Esta equação só funcionava para a luz visível de uma lâmpada de hidrogênio. Mas, mais tarde, a equação se tornou mais geral:
1 λ = R ( 1 m 2 - 1 n 2 ) , estilo de jogo 1 
onde R é a constante de Rydberg, igual a 0,0110 nm-1, e n deve ser maior que m.
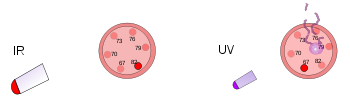
Introduzindo números diferentes para m e n, é fácil prever freqüências para muitos tipos de luz (ultravioleta, visível e infravermelha). Para ver como isto funciona, vá para a Hiperfísica e passe pelo meio da página. (Use H = 1 para hidrogênio).
Em 1908, Walter Ritz fez o princípio de combinação Ritz que mostra como certos intervalos entre freqüências continuam se repetindo. Isto se revelou importante para Werner Heisenberg vários anos mais tarde.
Em 1905, Albert Einstein utilizou a idéia de Planck para mostrar que um feixe de luz é composto por um fluxo de partículas chamado fótons. A energia de cada fóton depende de sua freqüência. A idéia de Einstein é o início da idéia na mecânica quântica de que todas as partículas subatômicas como elétrons, prótons, nêutrons e outras são ao mesmo tempo ondas e partículas. Isto levou a uma teoria sobre partículas subatômicas e ondas eletromagnéticas chamada dualidade onda-partícula. Aqui é onde partículas e ondas não eram uma nem a outra, mas tinham certas propriedades de ambas.
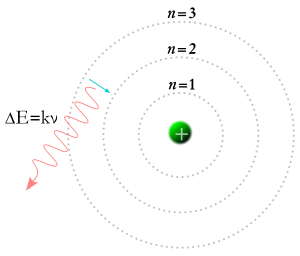
Em 1913, Niels Bohr teve a idéia de que os elétrons só poderiam assumir certas órbitas ao redor do núcleo de um átomo. Sob a teoria de Bohr, os números chamados m e n na equação acima poderiam representar órbitas. A teoria de Bohr dizia que os elétrons poderiam começar em alguma órbita m e terminar em alguma órbita n, ou um elétron poderia começar em alguma órbita n e terminar em alguma órbita m, então se um fóton atingir um elétron, sua energia será absorvida, e o elétron se moverá para uma órbita mais alta por causa dessa energia extra. Sob a teoria de Bohr, se um elétron cair de uma órbita mais alta para uma órbita mais baixa, então ele terá que desistir de energia na forma de um fóton. A energia do fóton será igual à diferença de energia entre as duas órbitas, e a energia de um fóton faz com que ele tenha uma certa freqüência e cor. A teoria de Bohr forneceu uma boa explicação de muitos aspectos dos fenômenos subatômicos, mas não respondeu porque cada uma das cores da luz produzida pelo hidrogênio incandescente (e pelo néon incandescente ou qualquer outro elemento) tem um brilho próprio, e as diferenças de brilho são sempre as mesmas para cada elemento.
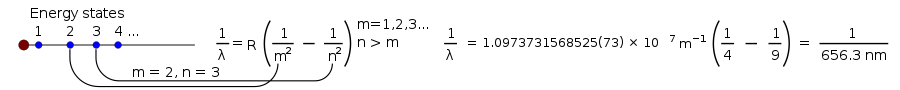
Na época em que Niels Bohr publicou sua teoria, a maioria das coisas sobre a luz produzida por uma lâmpada de hidrogênio eram conhecidas, mas os cientistas ainda não conseguiam explicar o brilho de cada uma das linhas produzidas pelo hidrogênio incandescente.
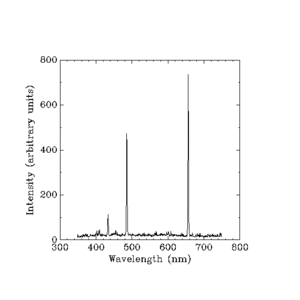
Werner Heisenberg assumiu a tarefa de explicar o brilho ou "intensidade" de cada linha. Ele não podia usar nenhuma regra simples como a que Balmer havia inventado. Ele teve que usar a matemática muito difícil da física clássica que calcula tudo em termos de coisas como a massa (peso) de um elétron, a carga (força elétrica estática) de um elétron, e outras pequenas quantidades. A física clássica já tinha respostas para o brilho das faixas de cor que uma lâmpada de hidrogênio produz, mas a teoria clássica dizia que deveria haver um arco-íris contínuo, e não quatro faixas de cor separadas. A explicação de Heisenberg é:
Há alguma lei que diz quais freqüências de hidrogênio incandescente produzirá. Ela tem que prever freqüências espaçadas quando os elétrons envolvidos estão se movendo entre órbitas próximas ao núcleo (centro) do átomo, mas também tem que prever que as freqüências se aproximarão cada vez mais enquanto observamos o que o elétron faz ao se mover entre órbitas cada vez mais distantes. Também terá que prever que as diferenças de intensidade entre as freqüências se aproximarão cada vez mais à medida que nos afastamos. Onde a física clássica já dá as respostas corretas por um conjunto de equações, a nova física tem que dar as mesmas respostas, mas por equações diferentes.
A física clássica usa os métodos do matemático francês Fourier para fazer uma imagem matemática do mundo físico, e usa coleções de curvas suaves que vão juntas para fazer uma curva suave que dá, neste caso, intensidades para a luz de todas as freqüências de alguma luz. Mas não é correto porque essa curva lisa só aparece em freqüências mais altas. Nas freqüências mais baixas, há sempre pontos isolados e nada liga os pontos. Assim, para fazer um mapa do mundo real, Heisenberg teve que fazer uma grande mudança. Ele teve que fazer algo para escolher apenas os números que correspondessem ao que era visto na natureza. Às vezes as pessoas dizem que ele "adivinhou" estas equações, mas ele não estava fazendo adivinhações cegas. Ele encontrou o que precisava. Os números que ele calculava colocariam pontos em um gráfico, mas não haveria nenhuma linha traçada entre os pontos. E fazer um "gráfico" apenas de pontos para cada conjunto de cálculos teria desperdiçado muito papel e não teria conseguido fazer nada. Heisenberg encontrou uma maneira de prever eficientemente as intensidades para diferentes freqüências e de organizar essas informações de uma maneira útil.
Apenas usando a regra empírica dada acima, aquela que Balmer iniciou e Rydberg melhorou, podemos ver como obter um conjunto de números que ajudaria Heisenberg a obter o tipo de imagem que ele queria:
A regra diz que quando o elétron se move de uma órbita para outra, ou ganha ou perde energia, dependendo se ele está se afastando do centro ou se está mais próximo dele. Assim, podemos colocar estas órbitas ou níveis de energia como cabeçalhos ao longo do topo e do lado de uma grade. Por razões históricas, a órbita mais baixa é chamada n, e a próxima órbita é chamada n - a, depois vem n - b, e assim por diante. É confuso que eles usaram números negativos quando os elétrons estavam realmente ganhando energia, mas é assim que as coisas são.
Como a regra de Rydberg nos dá frequências, podemos usar essa regra para colocar em números, dependendo de para onde o elétron vai. Se o elétron começa em n e termina em n, então ele não foi realmente a lugar algum, então não ganhou energia e não perdeu energia. Portanto, a freqüência é 0. Se o elétron começa em n-a e termina em n, então ele caiu de uma órbita maior para uma órbita menor. Se o fizer, perde energia, e a energia que perde aparece como um fóton. O fóton tem uma certa quantidade de energia, e, e isso está relacionado a uma certa freqüência f pela equação e = h f. Assim, sabemos que uma certa mudança de órbita vai produzir uma certa freqüência de luz, f. Se o elétron começa em n e termina em n - a, isso significa que ele passou de uma órbita mais baixa para uma órbita mais alta. Isso só acontece quando um fóton de certa freqüência e energia vem de fora, é absorvido pelo elétron e lhe dá sua energia, e é isso que faz o elétron sair para uma órbita mais alta. Assim, para manter tudo fazendo sentido, escrevemos essa freqüência como um número negativo. Havia um fóton com uma certa freqüência e agora ele foi tirado.
Assim, podemos fazer uma grade como esta, onde f(a←b) significa a freqüência envolvida quando um elétron passa do estado de energia (órbita) b para o estado de energia a (Novamente, as seqüências olham para trás, mas esta é a forma como foram escritas originalmente):
Grade de f
| Estados Elétricos | n | n-a | n-b | n-c | .... | |
| n | f(n←n) | f(n←n-a) | f(n←n-b) | f(n←n-c) | ..... | |
| n-a | f(n-a←n) | f(n-a←n-a) | f(n-a←n-b) | f(n-a←n-c) | ..... | |
| n-b | f(n-b←n) | f(n-b←n-a) | f(n-b←n-b) | f(n-b←n-c) | ..... | |
| transição .... | ..... | ..... | ..... | ..... | | |
Heisenberg não fez as grades desta maneira. Ele apenas fez as contas que lhe permitiriam obter as intensidades que ele procurava. Mas para fazer isso, ele teve que multiplicar duas amplitudes (quão alta uma onda mede) para trabalhar a intensidade. (Na física clássica, intensidade igual a amplitude ao quadrado.) Ele fez uma equação de aparência estranha para lidar com este problema, escreveu o resto de seu trabalho, entregou-o a seu chefe e foi de férias. O Dr. Born olhou para sua equação engraçada e parecia um pouco louco. Ele deve ter se perguntado: "Por que Heisenberg me deu esta coisa estranha? Por que ele tem que fazer desta maneira?" Então ele percebeu que estava olhando para uma planta de algo que ele já conhecia muito bem. Ele estava acostumado a chamar a grade ou a mesa que podíamos escrever fazendo, por exemplo, toda a matemática para as freqüências, uma matriz. E a estranha equação de Heisenberg era uma regra para multiplicar duas delas juntas. Max Born era um matemático muito, muito bom. Ele sabia que como as duas matrizes (grades) sendo multiplicadas representavam coisas diferentes (como posição (x,y,z) e momento (mv), por exemplo), então quando você multiplica a primeira matriz pelo segundo você obtém uma resposta e quando você multiplica a segunda matriz pela primeira matriz você obtém outra resposta. Mesmo não conhecendo a matemática matricial, Heisenberg já via este problema das "respostas diferentes" e isso o incomodara. Mas o Dr. Born era um matemático tão bom que viu que a diferença entre a primeira multiplicação de matrizes e a segunda multiplicação de matrizes sempre envolveria a constante de Planck, h, multiplicada pela raiz quadrada da negativa, i. Assim, poucos dias após a descoberta de Heisenberg eles já tinham a matemática básica para o que Heisenberg gostava de chamar de "princípio da indeterminação". Por "indeterminado" Heisenberg significava que algo como um elétron não é simplesmente fixado até que seja fixado. É um pouco como uma água-viva que está sempre se espremendo e não pode estar "em um só lugar", a menos que você a mate. Mais tarde, as pessoas adquiriram o hábito de chamá-lo de "princípio da incerteza de Heisenberg", o que fez muitas pessoas cometerem o erro de pensar que elétrons e coisas assim estão realmente "em algum lugar", mas nós temos dúvidas sobre isso em nossas próprias mentes. Essa idéia é errada. Não era sobre isso que Heisenberg estava falando. Ter problemas para medir algo é um problema, mas não é o problema do qual Heisenberg estava falando.
A idéia de Heisenberg é muito difícil de entender, mas podemos torná-la mais clara com um exemplo. Primeiro, vamos começar a chamar estas grades de "matrizes", porque em breve precisaremos falar sobre multiplicação de matrizes.
Suponha que comecemos com dois tipos de medidas, posição (q) e momento (p). Em 1925, Heisenberg escreveu uma equação como esta:
Y ( n , n - b ) = ∑ a p ( n , n - a ) q ( n - a , n - b ) {\i1}displaystyle Y(n,n-b)==sum _{a}^{},p(n,n-a)q(n-a,n-b)}  (Equação para a dinâmica e posição das variáveis conjugadas)
(Equação para a dinâmica e posição das variáveis conjugadas)
Ele não sabia, mas esta equação dá um plano para escrever duas matrizes (grades) e para multiplicá-las. As regras para multiplicar uma matriz por outra são um pouco confusas, mas aqui estão as duas matrizes de acordo com o plano, e depois o produto delas:
Matriz de p
| Estados Elétricos | n-a | n-b | n-c | .... | |
| n | p(n←n-a) | p(n←n-b) | p(n←n-c) | ..... | |
| n-a | p(n-a←n-a) | p(n-a←n-b) | p(n-a←n-c) | ..... | |
| n-b | p(n-b←n-a) | p(n-b←n-b) | p(n-b←n-c) | ..... | |
| transição .... | ..... | ..... | ..... | ..... | |
Matriz de q
| Estados Elétricos | n-b | n-c | n-d | .... | |
| n-a | q(n-a←n-b) | q(n-a←n-c) | q(n-a←n-d) | ..... | |
| n-b | q(n-b←n-b) | q(n-b←n-c) | q(n-b←n-d) | ..... | |
| n-c | q(n-c←n-b) | q(n-c←n-c) | q(n-c←n-d) | ..... | |
| transição .... | ..... | ..... | ..... | ..... | |
A matriz para o produto das duas matrizes acima conforme especificado pela equação relevante no papel de Heisenberg de 1925 é:
| Estados Elétricos | n-b | n-c | n-d | ..... |
| n | A | ..... | ..... | ..... |
| n-a | ..... | B | ..... | ..... |
| n-b | ..... | ..... | C | ..... |
Onde:
A=p(n←n-a)*q(n-a←n-b)+p(n←n-b)*q(n-b←n-b)+p(n←n-c)*q(n-c←n-b)+ .....
B=p(n-a←n-a)*q(n-a←n-c)+p(n-a←n-b)*q(n-b←n-c)+p(n-a←n-c)*q(n-c←n-c)+ .....
C=p(n-b←n-a)*q(n-a←n-d)+p(n-b←n-b)*q(n-b←n-d)+p(n-b←n-c)*q(n-d←n-d)+ .....
e assim por diante.
Se as matrizes fossem invertidas, o resultado seriam os seguintes valores:
A=q(n←n-a)*p(n-a←n-b)+q(n←n-b)*p(n-b←n-b)+q(n←n-c)*p(n-c←n-b)+.....
B=q(n-a←n-a)*p(n-a←n-c)+q(n-a←n-b)*p(n-a←n-b)*p(n-b←n-c)+q(n-a←n-c)*p(n-c←n-c)+.....
C=q(n-b←n-a)*p(n-a←n-d)+q(n-b←n-b)*p(n-b←n-d)+q(n-b←n-c)*p(n-d←n-d)+ .....
e assim por diante.
Observe como a mudança da ordem de multiplicação muda os números, passo a passo, que são realmente multiplicados.