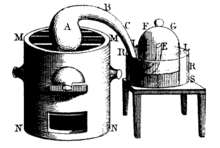
Experimentos iniciais
Uma das primeiras experiências conhecidas sobre como a combustão necessita de ar foi realizada pelo grego Philo de Byzantium no século II a.C. Ele escreveu em sua obra Pneumatica que virar um vaso de cabeça para baixo sobre uma vela acesa e colocar água ao redor desse vaso significava que alguma água entrava no vaso. Philo pensava que isto se devia ao fato de o ar ter sido transformado no clássico elemento fogo. Isto estava errado. Muito tempo depois, Leonardo da Vinci descobriu corretamente que o ar era consumido quando a combustão acontecia, o que forçou a entrada de água no vaso.
No final do século XVII, Robert Boyle descobriu que o ar é necessário para a combustão. O químico inglês John Mayow acrescentou a isso, mostrando que o fogo só precisava de uma parte de ar. Chamamos agora este oxigênio (na forma de dio-oxigênio). Em uma de suas experiências, ele descobriu que colocar uma vela em um recipiente fechado fazia com que a água subisse para substituir um quarto do volume do ar no recipiente, antes de sair. A mesma coisa aconteceu quando um rato foi colocado dentro da caixa. A partir disto, ele descobriu que o oxigênio é utilizado para a respiração e combustão.
Teoria do clogistão
Robert Hooke, Ole Borch, Mikhail Lomonosov e Pierre Bayen fizeram oxigênio em experiências nos séculos XVII e XVIII. Nenhum deles pensou que se tratasse de um elemento químico. Isto foi provavelmente por causa da idéia da teoria do clogistão. Isto era o que a maioria das pessoas acreditava que causava combustão e corrosão.
J. J. Becher inventou-o no ano de 1667, e Georg Ernst Stahl acrescentou-lhe em 1731. A teoria do phlogiston declarou que todos os materiais combustíveis eram feitos de duas partes. Uma parte, chamada de phlogiston, foi liberada quando a substância que a continha foi queimada.
Pensava-se que materiais muito combustíveis que deixam apenas uma pequena quantidade de resíduos, como madeira ou carvão, eram feitos de phlogiston. Coisas que corroem, como o ferro, foram pensadas para conter apenas uma pequena quantidade. O ar não fazia parte desta teoria.
Descoberta
O alquimista, filósofo e médico polonês Michael Sendivogius falou sobre uma substância no ar, chamando-a de "alimento da vida", e essa substância é o oxigênio. Sendivogius descobriu, entre os anos de 1598 e 1604, que a substância é a mesma que é feita durante a decomposição térmica do nitrato de potássio. Algumas pessoas acreditam que esta foi a descoberta do oxigênio, enquanto outras discordam.
Também se diz com freqüência que o oxigênio foi descoberto pela primeira vez pelo farmacêutico sueco Carl Wilhelm Scheele. Ele fabricou oxigênio aquecendo óxido de mercúrio e alguns nitratos em 1771. Scheele chamou o gás que ele fez de "ar de fogo", porque era o único gás conhecido que permitia a combustão. Ele publicou sua descoberta em 1777.
Em 1º de agosto de 1774, uma experiência realizada pelo clérigo britânico Joseph Priestley focalizou a luz solar no óxido de mercúrio em um tubo de vidro. Isto fez um gás que ele chamou de "ar dephlogisticated". Ele também descobriu que as velas queimavam mais brilhantemente no gás e os ratos viviam mais tempo enquanto o respiravam. Quando ele respirava o gás, ele dizia (simplificado) "Parecia ar normal, mas meus pulmões pareciam mais leves e fáceis depois". Suas descobertas foram publicadas em 1775. Como suas descobertas foram publicadas primeiro, costuma-se dizer que ele é o descobridor do oxigênio.
O químico francês Antoine Lavoisier disse mais tarde que também tinha descoberto a substância. O sacerdote o visitou em 1774 e lhe contou sobre sua experiência. Scheele também enviou uma carta a Lavoisier naquele ano, na qual falava de sua descoberta.
Contribuição da Lavoisier
Lavoisier realizou as primeiras experiências principais sobre oxidação e deu a primeira explicação correta sobre como funciona a combustão. Ele usou estes e outros experimentos para provar que a teoria do clogistão estava errada. Ele também tentou provar que a substância descoberta por Priestley e Scheele era um elemento químico.
Em uma experiência, Lavoisier descobriu que não houve aumento de massa quando o estanho e o ar eram aquecidos em um recipiente fechado. Ele também descobriu que o ar entrava correndo quando o contêiner era aberto. Depois disso, ele descobriu que a lata havia aumentado em massa na mesma quantidade que o ar que entrava correndo. Ele publicou suas descobertas em 1777. Ele escreveu que o ar era composto de dois gases. Um ele chamou de "ar vital" (oxigênio), que é necessário para a combustão e a respiração. O outro ele chamou de "azoto" (nitrogênio), que significa "sem vida" na língua grega. Este ainda é o nome de nitrogênio em alguns idiomas, inclusive o francês.
Lavoisier renomeou "ar vital" para "oxygène", que significa "produtor de ácidos" em grego. Ele chamou isto porque pensava que o oxigênio estava em todos os ácidos, o que estava errado. Muitos químicos perceberam que Lavoiser estava errado em seu nome, mas o nome já era comum demais para mudar.
"Oxygen" tornou-se o nome na língua inglesa, apesar de os cientistas ingleses serem contra.
História posterior
A teoria dos átomos de John Dalton dizia que todos os elementos tinham um átomo e que os átomos nos compostos geralmente estavam sozinhos. Por exemplo, ele pensou erroneamente que a água (H2O) tinha a fórmula de apenas HO. Em 1805, Joseph Louis Gay-Lussac e Alexander von Humboldt mostraram que a água é composta de dois átomos de hidrogênio e um átomo de oxigênio. Em 1811, Amedeo Avogadro calculou corretamente de que era feita a água, com base na lei de Avogadro.
No final do século XIX, os cientistas descobriram que o ar podia ser transformado em um líquido e que os compostos nele contidos podiam ser isolados por meio de compressão e resfriamento. O químico e físico suíço Raoul Pictet descobriu o oxigênio líquido ao evaporar o dióxido de enxofre para transformar o dióxido de carbono em um líquido. Isto também foi evaporado para resfriar o gás de oxigênio a fim de transformá-lo em um líquido. Ele enviou um telegrama para a Academia Francesa de Ciências em 22 de dezembro de 1877 contando-lhes sua descoberta.