Ácido
O artigo sobre certas propriedades dos bancos de dados está no ACID
Às vezes ácido é outro nome para a droga LSD (ácido lisérgico dietilamida)
Um ácido é uma substância que pode doar um íon de hidrogênio (H+) (geralmente falando, este será um próton) a outra substância. Os ácidos têm um pH inferior a 7,0. Um produto químico pode doar um próton se o átomo de hidrogênio estiver ligado a um átomo eletronegativo como oxigênio, nitrogênio ou cloro. Alguns ácidos são fortes e outros são fracos. Os ácidos fracos se agarram a alguns de seus prótons, enquanto os ácidos fortes soltam todos eles. Todos os ácidos liberam íons de hidrogênio em soluções. A quantidade de íons que são liberados por molécula irá determinar se o ácido é fraco ou forte. Ácidos fracos são ácidos que liberam parcialmente os átomos de hidrogênio que estão ligados. Estes ácidos, portanto, podem baixar o pH pela dissociação dos íons de hidrogênio, mas não completamente. Ácidos fracos geralmente têm um valor de pH de 4-6 enquanto ácidos fortes têm um valor de pH de 1 a 3.
Uma base é o "oposto químico" de um ácido. Uma base é uma substância que aceitará o átomo de hidrogênio do ácido. As bases são moléculas que podem se separar em água e liberar íons de hidróxido.

Ácido clorídrico (em béquer) reagindo com vapores de amônia para produzir cloreto de amônio (fumaça branca).
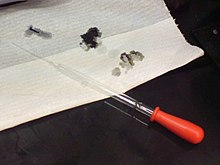
Os ácidos podem ser perigosos: Os furos no papel foram feitos por uma solução com 98% de ácido sulfúrico.
Como funcionam os ácidos
Ácidos e bases normalmente existem juntos em equilíbrio. Isto significa que dentro de uma amostra de um ácido, algumas moléculas desistirão de seus prótons e outras os aceitarão. Mesmo a água é uma mistura de um íon ácido, H3O+ (chamado íon hidronio) e um íon básico, OH- (chamado íon hidróxido). Um íon de hidrônio cederá seu próton a um íon de hidróxido, formando duas moléculas de H2O, que é neutro. Esta reação acontece continuamente em uma amostra de água, mas em geral a amostra é neutra porque há quantidades iguais de hidrônio e hidróxido na amostra. Para a maioria das reações, entretanto, os ácidos e bases não estão presentes em quantidades iguais, e este desequilíbrio é o que permite a ocorrência de uma reação química.
Todo ácido tem uma base conjugada formada pela remoção do próton do ácido. O ácido clorídrico (HCl), por exemplo, é um ácido e sua base conjugada é um ânion de cloro, ou Cl-. Um ácido e sua base conjugada são opostos em força. Como o HCl é um ácido forte, o Cl- é uma base fraca.
Imóveis
Os ácidos podem ter forças diferentes, alguns são mais reativos do que outros. Os ácidos mais reativos são muitas vezes mais perigosos.
Os ácidos podem ter muitas propriedades diferentes, dependendo de sua estrutura molecular. A maioria dos ácidos tem as seguintes propriedades:
- gosto azedo quando são comidos
- pode picar a pele quando são tocadas
- pode corroer (ou corroer) metais e pele
- pode ser usado como reagente durante a eletrólise, devido à presença de íons móveis
- virar papel litmus azul vermelho
- ficar vermelho ou laranja no indicador universal
- conduzir eletricidade
Os ácidos podem queimar a pele, a gravidade da queimadura dependendo do tipo e da concentração do ácido. Estas queimaduras químicas requerem atenção médica imediata.
Como os ácidos doam íons de hidrogênio, todos os ácidos devem ter hidrogênio neles.

Imagem de advertência utilizada com ácidos perigosos e bases perigosas. As bases são os opostos dos ácidos.
Importância
Os ácidos são importantes. Os ácidos nucleicos, como DNA e RNA, contêm o código genético. Estas moléculas determinam muitas características de um organismo, elas são passadas dos pais para os descendentes. O DNA contém os planos de como construir proteínas que são feitas de aminoácidos.
Os ácidos graxos e derivados de ácidos graxos são outro grupo de ácidos carboxílicos que desempenham um papel significativo na biologia. Estes contêm longas cadeias de hidrocarbonetos e um grupo de ácidos carboxílicos em uma extremidade. A membrana celular de quase todos os organismos é constituída principalmente por um bico fosfolipídeo, uma micela de cadeias de ácidos graxos hidrofóbicos com grupos de "cabeças" de fosfato polares e hidrofílicos.
Em humanos e em muitos outros animais, o ácido clorídrico é uma parte do ácido gástrico secretado dentro do estômago. Ele pode ajudar a hidrolisar proteínas e polissacarídeos. Ele também pode converter a pró-enzima inativa, pepsinogênio em enzima, pepsina. Alguns organismos produzem ácidos para defesa; por exemplo, formigas produzem ácido fórmico, e polvos produzem um ácido negro chamado magneta.
A maioria dos ácidos pode ser encontrada na natureza. Alguns deles incluem o seguinte:
- O vinagre é provavelmente um dos mais conhecidos; ele contém ácido acético, o que lhe confere seu sabor bem conhecido.
- Ácido nítrico, NHO3 é conhecido desde cerca do século XIII.
- Os ácidoscítricos, C6H8O7 podem ser encontrados em muitos tipos de frutas. Eles foram provavelmente descobertos pela Geber no século VIII.
- O ácido láctico C3H6O3 foi encontrado por Carl Wilhelm Scheele em 1780. Ele pode ser encontrado em produtos lácteos azedos, como o iogurte.
- O ácido sulfúrico H2SO4 foi provavelmente descoberto por Geber. Hoje, ele pode ser encontrado em baterias.
Páginas relacionadas
- Alkali
- Ácido fólico
Perguntas e Respostas
P: O que é o ACID?
R: O ACID é um artigo sobre certas propriedades de bancos de dados.
P: O que é ácido em geral?
R: Ácido em geral é uma substância que pode doar um íon de hidrogênio (H+) a outra substância, com um pH inferior a 7,0.
P: Quais são as condições sob as quais um produto químico pode doar um próton?
R: Um produto químico pode doar um próton se o átomo de hidrogênio estiver ligado a um átomo eletronegativo como oxigênio, nitrogênio, ou cloro.
P: Qual é a diferença entre ácidos fortes e ácidos fracos?
R: Ácidos fortes soltam todos os seus prótons, enquanto ácidos fracos se agarram a alguns deles. A quantidade de íons que são liberados por molécula determinará se o ácido é fraco ou forte.
P: Qual é a faixa de pH dos ácidos fracos e dos ácidos fortes?
R: Ácidos fracos geralmente têm um valor de pH de 4-6, enquanto ácidos fortes têm um valor de pH de 1 a 3.
P: O que é uma base?
R: Uma base é o "oposto químico" de um ácido. Uma base é uma substância que aceitará o átomo de hidrogênio do ácido. As bases são moléculas que podem se separar em água e liberar íons de hidróxido.
P: O que é LSD?
R: O LSD (ácido lisérgico dietilamida) é uma droga que às vezes é chamada de ácido, mas não está relacionado com o ácido mencionado neste artigo.
Pesquise na enciclopédia