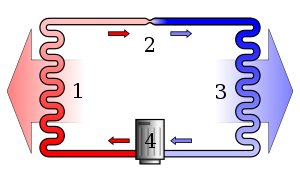
A segunda lei da termodinâmica diz que quando a energia muda de uma forma para outra, ou a matéria se move livremente, a entropia (desordem) em um sistema fechado aumenta.
As diferenças de temperatura, pressão e densidade tendem a nivelar horizontalmente após algum tempo. Devido à força da gravidade, a densidade e a pressão nem mesmo na vertical. A densidade e a pressão na parte inferior serão mais do que na parte superior.
A entropia é uma medida de propagação de matéria e energia para todos os lugares a que eles têm acesso.
A formulação mais comum para a segunda lei de termodinâmica é essencialmente devido a Rudolf Clausius:
Em outras palavras, tudo tenta manter a mesma temperatura ao longo do tempo.
Há muitas declarações da segunda lei que usam termos diferentes, mas todas significam a mesma coisa. Outra declaração de Clausius é:
O calor não pode por si só passar de um corpo mais frio para um corpo mais quente.
Uma declaração equivalente de Lord Kelvin é:
Uma transformação cujo único resultado final é a conversão de calor, extraído de uma fonte a temperatura constante, em trabalho, é impossível.
A segunda lei só se aplica aos grandes sistemas. A segunda lei é sobre o comportamento provável de um sistema onde nenhuma energia ou matéria entra ou sai. Quanto maior for o sistema, maior será a probabilidade de a segunda lei ser verdadeira.
Perguntas e Respostas
P: O que é a segunda lei da termodinâmica?
R: A segunda lei da termodinâmica afirma que quando a energia muda de uma forma para outra, ou a matéria se move livremente, a entropia (desordem) em um sistema fechado aumenta.
P: O que tende a se equilibrar horizontalmente com o tempo?
R: As diferenças de temperatura, pressão e densidade tendem a se nivelar horizontalmente depois de algum tempo.
P: Por que a densidade e a pressão não se nivelam verticalmente?
R: Devido à força da gravidade, a densidade e a pressão não se igualam verticalmente. A densidade e a pressão na parte inferior serão maiores do que na parte superior.
P: O que é entropia?
R: Entropia é uma medida da dispersão de matéria e energia em todos os lugares a que têm acesso.
P: Qual é a formulação mais comum para a segunda lei da termodinâmica?
R: A formulação mais comum para a segunda lei da termodinâmica deve-se essencialmente a Rudolf Clausius: tudo tenta manter a mesma temperatura ao longo do tempo.
P: Qual é outra afirmação de Clausius com relação à segunda lei da termodinâmica?
R: Outra afirmação de Clausius é que o calor não pode, por si só, passar de um corpo mais frio para um mais quente.
P: A que tipo de sistema se aplica a segunda lei da termodinâmica?
R: A segunda lei da termodinâmica só se aplica a sistemas grandes, nos quais nenhuma energia ou matéria entra ou sai. Quanto maior for o sistema, maior a probabilidade de a segunda lei ser verdadeira.