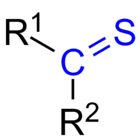
Um thioketone (ou thione) é qualquer molécula com o grupo R2C=S. É como uma cetona com o átomo de oxigênio trocado com um de enxofre. O átomo de enxofre tem uma dupla ligação com o átomo de carbono. Ele também mantém dois pares solitários.
As tiocetonas são muito reativas. Isto porque eles são bons eletrofílicos. Muitos deles são instáveis. Eles querem formar anéis. Eles fazem isso com reações de cicloadição, semelhantes à reação Diels-Alder.
Se um dos grupos R é hidrogênio, a molécula é a versão de enxofre de um aldeído. É chamado de thial, e é ainda mais reativo que um thioketone.