O calor pode fazer com que os laços duplos formem um anel. As condições cíclicas térmicas geralmente têm (4n + 2) π elétrons participando do material de partida, para algum número inteiro, n. Devido à simetria orbital, a maioria das condições cíclicas são suprafaciais-suprafaciais. Raramente, são antarafaciais-antarafaciais. Há alguns exemplos de cácloadições térmicas que têm 4n π elétrons (por exemplo, a [2 + 2] cácloadição). Estes procedem num sentido suprafacial-antarafacial. Por exemplo, a dimerização do ceteno tem um conjunto ortogonal de p orbitais. Essas orbitais p permitem que a reação prossiga usando um estado de transição cruzado.
A luz também pode fazer com que os laços duplos formem um anel. Cicloadições nas quais participam 4n π elétrons também podem ocorrer como resultado da ativação fotoquímica. Aqui, um componente faz com que um elétron passe do orbital molecular ocupado mais alto (HOMO) (π ligação) para o orbital molecular desocupado mais baixo (LUMO) (π* anti-ligação). Depois que o elétron é promovido para o orbital superior, a simetria orbital permite que a reação prossiga de forma suprafacial-suprafacial. Um exemplo é a reação DeMayo. Outro exemplo é mostrado abaixo, a dimerização fotoquímica do ácido cinâmico.
Note que nem todas as ciclizações fotoquímicas (2+2) são condições cíclicas; algumas são conhecidas por operar por mecanismos radicais.
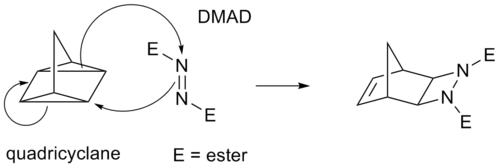
Alguns títulos ciclopropânicos em vez de π funcionam através de anéis ciclopropânicos tensos; como estes têm um caráter significativo π. Por exemplo, um análogo para a reação Diels-Alder é a reação quadriciclane-DMAD:
Na notação (i+j+...) de condição cíclica i e j referem-se ao número de átomos envolvidos na condição cíclica. Nesta notação, uma reação Diels-Alder é uma (4+2)cicloadição e uma adição 1,3-dipolar como o primeiro passo na ozonólise é uma (3+2)cicloadição. Esta notação usa parênteses. A notação preferida pela IUPAC, entretanto, com [i+j+...] conta os elétrons e não os átomos. Ela usa parênteses rectos. Nesta notação, a reação Diels-Alder e a reação dipolar tornam-se ambas uma [4+2] condição cíclica. A reação entre norbornadieno e um alkyne ativado é uma condição cíclica [2+2+2].
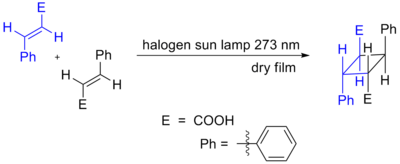
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)