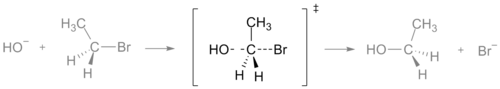Em uma reação química, o estado de transição é o ponto onde há um valor máximo de energia. Esta energia é chamada de energia de ativação. Quando duas ou mais moléculas são misturadas, elas se tocam uma na outra. Se elas atingirem com energia suficiente para passar pelo estado de transição, elas reagirão e formarão novas moléculas. No estado de transição, novos laços são formados enquanto os antigos são quebrados. Em um gráfico ou desenho, o estado de transição é freqüentemente marcado com o símbolo da adaga dupla ‡.
É muito difícil estudar um estado de transição. Isto porque é tão alto em energia que as moléculas permanecerão nessa forma por um tempo muito curto, geralmente em femtossegundos. É importante não confundir os estados de transição com os intermediários. Os intermediários são encontrados em pontos mínimos de energia e podem viver por um tempo muito longo. Como um estado de transição, porém, um intermediário está entre os reagentes e os produtos de uma reação.
O estudo dos estados de transição é muito importante para compreender os mecanismos de reação. Há teorias e programas de computador que podem ser usados para calcular como se parece o estado de transição. Isto é uma parte da cinética química.