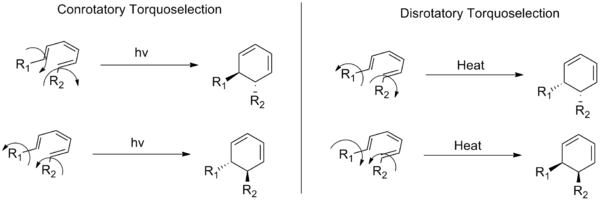
Estes termos descrevem duas classes de uma reação eletrociclica (um tipo de reação química orgânica). Em modo conrotatório, os substitutos localizados nas extremidades de um sistema conjugado de dupla ligação se movem no mesmo sentido (horário ou anti-horário) durante a abertura ou fechamento do anel. No modo desrotatório, eles se movem em direções opostas.
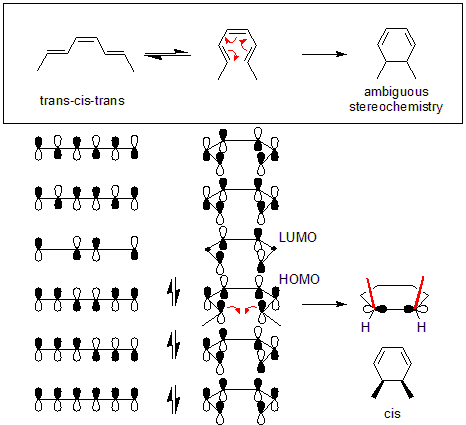
Um exemplo é a conversão do trans-cis-trans-2,4,6-octatriene em cis-dimetilciclohexadieno (topo da figura). A mecânica orbital da reação precisa de um modo desrotatório. A simetria orbital do octatrieno orbital molecular mais alto ocupado (HOMO) requer que os orbitais pi pi finais se movam em direções opostas para formar a simetria correta encontrada na ligação sigma.
Os rearranjos térmicos de todos os sistemas conjugados contendo 4n + 2 pi de elétrons são estereo-específicos. Isto é baseado na preservação da simetria orbital no orbital molecular mais ocupado. Sistemas contendo elétrons de 4n pi mostram o modo oposto conrotatório. Isto também é verdade para rearranjos de 4n + 2 pi (onde n é um número inteiro) elétrons movidos pela luz (fotoinduzidos). Os rearranjos fotoinduzidos de sistemas de elétrons 4n pi (onde o número de elétrons é divisível por 4) seguem a regra desrotatória.
As regras da Woodward-Hoffmann resumem as diferentes reações acima.
A figura a seguir também mostra a diferença entre as reações conrotatórias e disrotatórias: