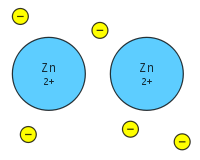
Uma ligação metálica é a partilha de muitos elétrons destacados entre muitos íons positivos, onde os elétrons atuam como uma "cola", dando à substância uma estrutura definida. É diferente da colagem covalente ou iônica. Os metais têm baixa energia de ionização. Portanto, os elétrons de valência podem ser deslocados através dos metais. Os elétrons deslocalizados não estão associados a um núcleo particular de um metal, ao invés disso, eles são livres para se mover por toda a estrutura cristalina formando um "mar" de elétrons.
Os elétrons e os íons positivos no metal têm uma forte força de atração entre eles. Portanto, os metais freqüentemente têm um alto ponto de fusão ou de ebulição. O princípio é semelhante ao das ligações iônicas.
As ligações metálicas causam muitas das características dos metais, tais como força, maleabilidade, ductilidade, brilho, condução de calor e eletricidade.
Como os elétrons se movimentam livremente, o metal tem alguma condutividade elétrica. Ele permite que a energia passe rapidamente através dos elétrons, gerando uma corrente elétrica. Os metais conduzem calor pelo mesmo motivo: os elétrons livres podem transferir a energia a uma velocidade mais rápida do que outras substâncias com elétrons que estão fixados na posição. Há também poucos não metálicos que conduzem eletricidade: grafite (porque, como os metais, tem elétrons livres) e compostos iônicos que são fundidos ou dissolvidos na água, que têm íons em movimento livre.
As ligações metálicas têm pelo menos um elétron de valência que não compartilham com átomos vizinhos, e não perdem elétrons para formar íons. Ao invés disso, os níveis de energia externa (orbitais atômicos) dos átomos metálicos se sobrepõem. Eles são semelhantes às ligações covalentes. Nem todos os metais exibem ligação metálica. Por exemplo, os íons de mercúrio (Hg2+
2) formar ligações metal-metal covalentes.
Uma liga é uma solução de metais. A maioria das ligas são brilhantes como os metais puros são.