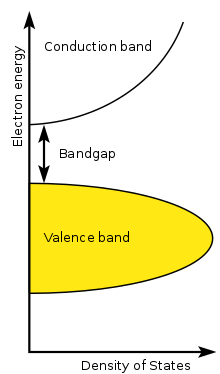
Os cientistas usam a abertura da banda para prever se um sólido conduzirá a eletricidade. A maioria dos elétrons (chamados de elétrons de valência) são atraídos para o núcleo de apenas um átomo. Mas se um elétron tem energia suficiente para voar para longe de seu núcleo mais próximo, ele pode se juntar ao fluxo de corrente elétrica através dos muitos átomos que compõem o sólido. Os elétrons que não estão firmemente presos a apenas um núcleo são chamados de banda condutora.
Em semicondutores e isoladores, a mecânica quântica mostra que os elétrons são encontrados apenas em uma série de faixas de energia. Os elétrons são proibidos a partir de outros níveis de energia. O termo intervalo de banda refere-se à diferença de energia entre a parte superior da banda de valência e a parte inferior da banda de condução. Os elétrons são capazes de saltar de uma banda para outra. Entretanto, um elétron precisa de uma certa quantidade de energia para saltar de uma banda de valência para uma banda de condução. A quantidade de energia necessária difere com diferentes materiais. Os elétrons podem ganhar energia suficiente para pular para a banda de condução absorvendo um fone (calor) ou um fóton (luz).
Um semicondutor é um material com um pequeno mas não nulo intervalo de banda que se comporta como isolante à temperatura zero absoluta (0 K), mas permite que o calor excite elétrons o suficiente para saltar em sua banda condutora a temperaturas abaixo de seu ponto de fusão. Em contraste, um material com uma grande abertura de banda é um isolante. Em condutores, as bandas de valência e de condução podem se sobrepor, de modo que podem não ter uma folga de banda.
A condutividade dos semicondutores intrínsecos é fortemente dependente da folga da banda. Os únicos suportes disponíveis para a condução são os elétrons que têm energia térmica suficiente para serem excitados através da fenda da banda.
A engenharia de abertura de banda é o processo de controlar ou alterar a abertura de banda de um material através do controle da composição de certas ligas semicondutoras, tais como GaAlAs, InGaAs, e InAlAs. Também é possível construir materiais em camadas com composições alternadas por técnicas como a epitaxia de feixe molecular. Estes métodos são utilizados no projeto de transistores bipolares heterojuncionais (HBTs), díodos laser e células solares.
É difícil traçar uma linha entre os semicondutores e os isoladores. Uma maneira é pensar nos semicondutores como um tipo de isolante com uma estreita abertura de banda. Isoladores com um espaço de banda maior, geralmente maior que 3 eV,[fonte? ] não são colocados no grupo semicondutor e geralmente não exibem comportamento semicondutor sob condições práticas. A mobilidade eletrônica também desempenha um papel na determinação do agrupamento informal de um material como um semicondutor.
A energia da abertura de banda dos semicondutores tende a diminuir com o aumento da temperatura. Quando a temperatura aumenta, a amplitude das vibrações atômicas aumenta, levando a um maior espaçamento interatômico. A interação entre os fones de malha e os elétrons e furos livres também afetará um pouco a folga da banda. A relação entre a energia da abertura da banda e a temperatura pode ser descrita pela expressão empírica de Varshni,
 onde Eg(0), α e β são constantes materiais.
onde Eg(0), α e β são constantes materiais.
Em um cristal semicondutor normal, a abertura da banda é fixa devido a estados de energia contínua. Em um cristal de ponto quântico, o intervalo de banda é dependente do tamanho e pode ser alterado para produzir uma gama de energias entre a banda de valência e a banda de condução. Também é conhecido como efeito de confinamento quântico.
As fendas das bandas também dependem da pressão. As aberturas de banda podem ser diretas ou indiretas, dependendo da estrutura da banda eletrônica.
Interpretação matemática
Classicamente, a razão de probabilidades de que dois estados com uma diferença de energia ΔE serão ocupados por um elétron é dada pelo fator Boltzmann:
e ( - Δ E k T ) Estilo de jogo e^{\i1}esquerda(frac {\i}}delta E^direita(kT) 
onde:
- e é o número de Euler (a base dos logaritmos naturais)
- ΔE é a diferença de energia
- k é a constante de Boltzmann
- T é a temperatura.
No nível Fermi (ou potencial químico), a probabilidade de um estado ser ocupado é ½. Se o nível Fermi estiver no meio de uma fenda de 1 eV, esta probabilidade é e-20 ou cerca de 2,0⋅10-9 na energia térmica de 25,9 meV em temperatura ambiente.
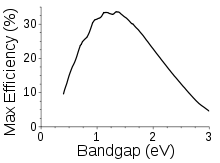
Células fotovoltaicas
Os elétrons podem ser excitados tanto pela luz quanto pelo calor. A abertura da banda determina que parte do espectro solar uma célula fotovoltaica absorve. Um conversor solar luminescente utiliza um meio luminescente para downconverter fótons com energias acima do intervalo de banda para energias fotônicas mais próximas do intervalo de banda do semicondutor que compreende a célula solar.
Lista de lacunas de banda
| Material | Símbolo | Abertura de banda (eV) @ 302K | Referência |
| Silício | Si | 1.11 | |
| Selênio | Se | 1.74 | |
| Germanium | Ge | 0.67 | |
| Carboneto de silício | SiC | 2.86 | |
| Fosforeto de alumínio | AlP | 2.45 | |
| Arsenieto de alumínio | AlAs | 2.16 | |
| Antimonido de alumínio | AlSb | 1.6 | |
| Nitreto de alumínio | AlN | 6.3 | |
| Diamante | C | 5.5 | |
| Fosforeto de gálio(III) | GaP | 2.26 | |
| Gálio(III) arsenieto | GaAs | 1.43 | |
| Nitreto de gálio(III) | GaN | 3.4 | |
| Sulfureto de gálio(II) | GaS | 2.5 | |
| Antimonido de gálio | GaSb | 0.7 | |
| Antimonido de índio | InSb | 0.17 | |
| Nitreto de índio(III) | InN | 0.7 | |
| Fosforeto de índio(III) | InP | 1.35 | |
| Arsenieto de índio(III) | InAs | 0.36 | |
| Dissilicida de ferro | β-FeSi2 | 0.87 | |
| Óxido de zinco | ZnO | 3.37 | |
| Sulfeto de zinco | ZnS | 3.6 | |
| Selenida de zinco | ZnSe | 2.7 | |
| Telureto de zinco | ZnTe | 2.25 | |
| Sulfeto de cádmio | CdS | 2.42 | |
| Selenieto de cádmio | CdSe | 1.73 | |
| Telureto de cádmio | CdTe | 1.49 | |
| Sulfureto de chumbo(II) | PbS | 0.37 | |
| Selenide de chumbo(II) | PbSe | 0.27 | |
| Telluride de chumbo(II) | PbTe | 0.29 | |
| Óxido de cobre(II) | CuO | 1.2 | |
| Óxido de cobre(I) | Cu2O | 2.1 | |