Termodinâmica
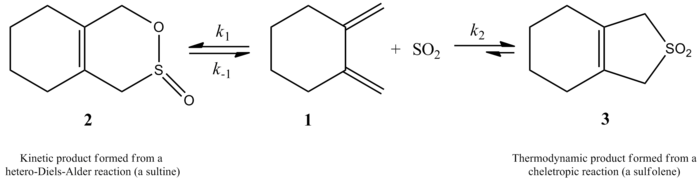
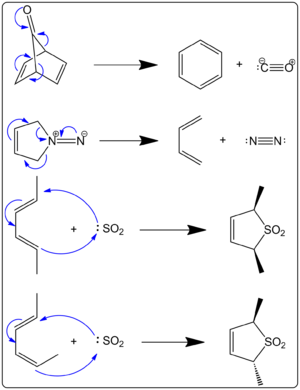
Quando o dióxido de enxofre reage com butadieno e isopreno, resultam dois produtos diferentes. O mecanismo de reação controlará o que for feito. Um produto cinético e um produto termodinâmico são ambos possíveis. Mais do produto termodinâmico é feito do que o produto cinético. O produto cinético vem de uma reação Diels-Alder, enquanto que uma reação queltropica faz um produto mais estável termodinamicamente. A via queltropica é mais utilizada porque torna mais estável o adutor de anéis com cinco membros. O esquema abaixo mostra a diferença entre os dois produtos. O caminho para a esquerda mostra o produto termodinâmico, enquanto o caminho para a direita mostra o produto cinético. Suarez e Sordo mostraram isto em 1995. Eles mostraram isto ambos com experimentos e utilizando cálculos gaussianos.
Cinética
Um exemplo disso são as reações queltropicais de 1,3 dienos com dióxido de enxofre. Os químicos analisaram cuidadosamente a cinética desta reação. Em 1976, Isaacs e Laila mediram os fatores quenéticos para a adição de dióxido de enxofre aos derivados de butadieno. As taxas de adição foram monitoradas em benzeno a 30 °C com um excesso inicial de vinte vezes mais dieno. Eles usaram um espectrofotômetro para estudar a luz a 320 nm para medir o desaparecimento de SO2. A reação mostrou uma "pseudo cinética de primeira ordem". Os químicos descobriram que os grupos de retirada de elétrons sobre o dieno diminuíram a taxa de reação. Além disso, a taxa de reação foi afetada consideravelmente pelos efeitos estéreis de 2-substituintes, com grupos mais volumosos aumentando a taxa de reação. (Em outras palavras, quanto maior o grupo de átomos pendurados no segundo átomo de carbono, mais rapidamente a reação funcionava). Os autores atribuem isto à tendência dos grupos volumosos de favorecer a conformação cisoide do dieno, essencial para a reação (ver tabela abaixo). Além disso, as taxas a quatro temperaturas foram medidas para sete dos dienos. A partir destas medidas, os químicos utilizaram a equação de Arrhenius para calcular a entalpia de ativação (ΔH‡) e entropia de ativação (ΔS‡) para cada reação. Este foi um dos primeiros esforços importantes para estudar a cinética de uma reação queltropical.
| -Butadieno | 104 k /min-1 (30 °C) (± 1-2%) absoluto | 104 k /min-1 (30 °C) (± 1-2%) relativo | ΔH‡ /kcal mol-1 | ΔS‡ /cal mol-1 K-1 |
| 2-metil | 1.83 | 1.00 | 14.9 | -15 |
| 2-etil | 4.76 | 2.60 | 10.6 | -20 |
| 2-isopropil | 13.0 | 7.38 | 12.5 | -17 |
| 2-tert-butílico | 38.2 | 20.8 | 10.0 | -19 |
| 2-neopentyl | 17.2 | 9.4 | 11.6 | -18 |
| 2-cloro | 0.24 | 0.13 | N/A | N/A |
| 2-bromoethyl | 0.72 | 0.39 | N/A | N/A |
| 2-p-tolyl | 24.7 | 13.5 | 10.4 | -19 |
| 2-fenil | 17.3 | 9.45 | N/A | N/A |
| 2-(p-bromofenil) | 9.07 | 4.96 | N/A | N/A |
| 2,3-dimetil | 3.54 | 1.93 | 12.3 | -18 |
| cis-1-metilo | 0.18 | 0.10 | N/A | N/A |
| trans-1-metilo | 0.69 | 0.38 | N/A | N/A |
| 1,2-dimetileno-ciclo-hexano | 24.7 | 13.5 | 11.4 | -16 |
| 2-metil-1,1,4,4-d4 | 1.96 | N/A | N/A | N/A |
Monnat, Vogel e Sordo, em 2002, mediram a cinética da adição de dióxido de enxofre a 1,2-dimetilidenecicloalcanos. Eles escreveram que a reação do 1,2-dimetilideneciclohexano com dióxido de enxofre pode dar dois produtos diferentes, dependendo das condições de reação. A reação faz a sultina correspondente através de uma reação hetero-Diels-Alder sob controle cinético (≤ -60 °C), mas, sob controle termodinâmico (≥ -40 °C), a reação faz o sulfoleno correspondente através de uma reação queltropical. A entalpia de ativação para a reação hetero-Diels-Alder é cerca de 2 kcal/mol menor que a correspondente reação queltropica. O sulfoleno é cerca de 10 kcal/mol mais estável do que a sultina isométrica na solução CH2Cl2/SO2.
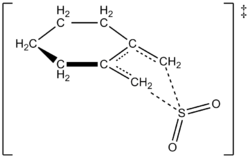
Os autores conseguiram elaborar experimentalmente uma lei de 261,2 K para a reação de 1,2-dimetilidenociclohexano com dióxido de enxofre para dar o sulfoleno correspondente. A reação foi de primeira ordem em 1,2-dimetilideneciclohexano, mas de segunda ordem em dióxido de enxofre (ver abaixo). Isto confirmou uma previsão de químicos teóricos baseada em cálculos ab initio quantum de alto nível. Usando métodos computacionais, os autores propuseram uma estrutura de transição para a reação queltropical do 1,2-dimetilideneciclohexano com dióxido de enxofre (ver figura à direita). A reação é de segunda ordem em dióxido de enxofre porque outra molécula de dióxido de enxofre provavelmente se liga ao estado de transição para ajudar a estabilizá-lo. Resultados semelhantes foram encontrados em um estudo de Suarez, Sordo e Sordo de 1995 que utilizou cálculos ab initio para estudar o controle cinético e termodinâmico da reação de dióxido de enxofre com 1,3-dieno.
d [ 3 ] d t = k 2 [ 1 ] [ S O 2 ] 2 {\frac {dt}}=k_{2}[1][SO_{2}]^{2}} 2 {\frac {dt}}=k_{2}[SO_{2}} ![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)
Efeitos do solvente
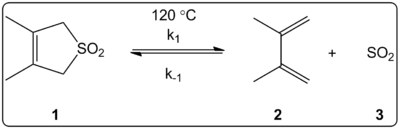
O efeito do solvente da reação queltropical de 3,4-dimetil-2,5-dihidrotiofen-1,1-dióxido (mostrado à direita) foi investigado cinicamente em 14 solventes. As constantes de taxa de reação da reação direta e reversa, além das constantes de equilíbrio, foram encontradas linearmente correlacionadas com a escala de polaridade do solvente ET(30).
As reações foram feitas a 120 °C e foram estudadas por espectroscopia de 1H-NMR da mistura de reação. Constatou-se que a taxa de avanço k1 diminuiu por um fator de 4,5, passando do ciclohexano para o metanol. Verificou-se que a taxa inversa k-1 aumentou por um fator de 53 passando do ciclohexano para o metanol, enquanto a constante de equilíbrio Keq diminuiu por um fator de 140. Sugere-se que há uma mudança da polaridade durante o processo de ativação como evidenciado pelas relações entre os dados de equilíbrio e cinéticos. Os autores dizem que a reação parece ser influenciada pela polaridade do solvente, e isto pode ser demonstrado pela mudança nos momentos dipolares quando se passa do estado reativo para o estado de transição para o produto. Os autores também afirmam que a reação queltropica não parece ser influenciada nem pela acidez do solvente nem pela basicidade.
Os resultados deste estudo levam os autores a esperar os seguintes comportamentos:
1. A mudança na polaridade do solvente influenciará a taxa menos do que o equilíbrio.
2. As constantes de taxa serão caracterizadas pelo efeito oposto na polaridade: k1 diminuirá ligeiramente com o aumento de ET(30), e k-1 aumentará sob as mesmas condições.
3. O efeito sobre o k-1 será maior que sobre o k1.

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)