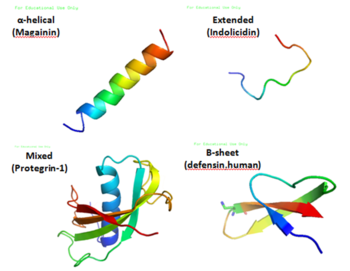
Os peptídeos de defesa do hospedeiro (ou peptídeos antimicrobianos) fazem parte da resposta imune inata. Eles são encontrados entre todas as classes de vida.
Eles atuam contra os microorganismos invasores. Os peptídeos matam bactérias Gram negativas e Gram positivas. Isto inclui as cepas resistentes aos antibióticos convencionais. Os peptídeos também atuam contra micobactérias (incluindo a Mycobacterium tuberculosis), vírus envolvidos, fungos e até mesmo células transformadas ou cancerosas.
Estes peptídeos são excelentes candidatos para uso médico. Eles complementam a terapia antibiótica convencional. Eles têm uma ampla gama de atividade, e são bactericidas em oposição a bacteriostáticos. Eles precisam apenas de um curto tempo de contato para matar as bactérias.
Há grandes diferenças entre as células procarióticas e eucarióticas como alvos para os peptídeos antimicrobianos. Estes peptídeos são antibióticos potentes e de amplo espectro. Ao contrário da maioria dos antibióticos, parece que os peptídeos antimicrobianos também podem melhorar a imunidade, trabalhando como imunomoduladores (fortalecendo o sistema imunológico).
Estrutura e propriedades gerais
Os peptídeos de defesa do hospedeiro são tipicamente curtos (≈12–50 aminoácidos), ricos em resíduos carregados positivamente (catiônicos) e com regiões anfipáticas (ou seja, com partes hidrofóbicas e hidrofílicas). Essas características favorecem a interação com superfícies microbianas carregadas negativamente e com membranas, diferenciando-as das membranas eucarióticas em muitos casos. Exemplos conhecidos incluem as defensinas (alfa e beta) e a catelicidina humana LL-37, além de peptídeos de anfíbios (como magaininas) e de insetos (cecropinas).
Mecanismos de ação
Os mecanismos são variados e muitas vezes múltiplos para um mesmo peptídeo:
- Disrupção de membrana: formação de poros ou desnaturação da bicamada lipídica por modelos conhecidos como "barrel-stave", "toroidal" ou "carpet". Isso leva à rápida lise celular.
- Alvo intracelular: alguns peptídeos atravessam a membrana e interferem em processos internos — inibindo a síntese de DNA/RNA, proteínas ou celulares, ou inibindo enzimas essenciais.
- Inibição de biofilmes: impedem formação de biofilmes ou promovem a dispersão de comunidades microbianas, o que é importante contra infecções crônicas.
- Neutralização de endotoxinas: muitos peptídeos ligam-se ao LPS (lipopolissacarídeo) bacteriano, reduzindo a inflamação exagerada associada à sepse.
Ação imunomoduladora
Além da atividade microbicida, esses peptídeos desempenham papéis-chave na modulação do sistema imune:
- atraem e ativam células do sistema imune (quimiotaxia de neutrófilos, monócitos e células dendríticas);
- modulam a produção de citocinas e quimiocinas, podendo reduzir respostas inflamatórias excessivas ou, quando necessário, amplificá-las;
- promovem a cicatrização de feridas, angiogênese e regeneração tecidual;
- interagem com receptores imunomediadores e influenciam a apresentação de antígenos e a ativação de células adaptativas.
Vantagens terapêuticas e aplicações
Por suas propriedades, os peptídeos antimicrobianos têm amplo potencial clínico:
- tratamentos tópicos (feridas infectadas, queimaduras, úlceras diabéticas);
- uso como adjuvantes de antibióticos tradicionais para ampliar o espectro ou reverter resistência;
- revestimentos antimicrobianos para dispositivos médicos e implantes;
- desenvolvimento de agentes anti-biofilme para infecções de cateteres e próteses;
- potencial na terapia antiviral e anticâncer, pela capacidade de destruir células infectadas ou transformadas e modular a resposta imune.
Limitações e desafios clínicos
Apesar do potencial, existem desafios a superar:
- Toxicidade e especificidade: alguns peptídeos podem ser hemolíticos ou tóxicos para células humanas em concentrações altas.
- Estabilidade: peptídeos naturais são susceptíveis à degradação por proteases no sangue e em tecidos.
- Custos de produção: síntese de peptídeos e formulações avançadas podem ser caros.
- Administração e entrega: alcançar concentrações efetivas no local da infecção sem efeitos sistêmicos indesejáveis exige estratégias de entrega (veículos, liberação controlada).
- Possibilidade de resistência: embora o aparecimento de resistência seja geralmente mais lento que para antibióticos clássicos, mecanismos como alteração da carga da membrana, secreção de proteases e formação de biofilme podem reduzir a eficácia.
Estratégias para superar barreiras
Para transformar peptídeos em medicamentos viáveis, pesquisadores usam várias abordagens:
- engenharia de peptídeos (substituição por D-aminoácidos, ciclagem, ancoragem lipídica) para aumentar estabilidade e reduzir degradação;
- desenvolvimento de peptidomiméticos e análogos sintéticos com propriedades semelhantes, mas maior resistência a proteases;
- formulações que protegem o peptídeo (lipossomas, nanopartículas, hidrogéis) e permitem liberação localizada;
- combinações com antibióticos convencionais para sinergia e menor probabilidade de resistência;
- uso tópico sempre que possível (reduz exposição sistêmica e degradação).
Estado do desenvolvimento e perspectivas
Alguns peptídeos e seus análogos já chegaram a ensaios clínicos e há um interesse crescente da indústria farmacêutica e acadêmica. Exemplos de aplicação clínica mais avançada incluem formulações tópicas para feridas e investigações em agentes anti-biofilme. A pesquisa atual foca em otimizar eficácia, segurança, custo e sistemas de entrega.
Conclusão
Os peptídeos de defesa do hospedeiro combinam ação microbicida rápida com capacidade imunomoduladora, tornando-os candidatos atraentes para novas terapias infecciosas e também para aplicação em imunoterapia e cicatrização. Avanços em biotecnologia, química de peptídeos e sistemas de liberação estão tornando cada vez mais viável a transição desses compostos do laboratório para usos clínicos, embora desafios de segurança, estabilidade e custo ainda precisem ser endereçados.