Os compostos organometálicos são compostos que possuem ligações químicas entre um ou mais átomos de metal e um ou mais átomos de carbono de um grupo organílico (um ligante orgânico). Eles têm o prefixo "organo-". (por exemplo, compostos organopalladium). Os compostos organometálicos incluem subgrupos como as metaloproteínas, como a hemoglobina.
O termo "metalorgânicos" geralmente se refere a compostos contendo metal que não possuem ligações direto metal-carbono, mas que contêm ligantes orgânicos que os ligam a um composto orgânico. Os beta-diketonatos de metal, alcóxidos e dialquilamidas são membros desta classe.
Além dos metais tradicionais, elementos como boro, silício, arsênico e selênio formam compostos organometálicos.
Compostos de coordenação com ligantes orgânicos
Muitos complexos têm laços de coordenação entre um ligante metálico e um orgânico. Os ligantes orgânicos geralmente ligam o metal através de uma heteroatomia como oxigênio ou nitrogênio, caso em que tais compostos são chamados de "compostos de coordenação".
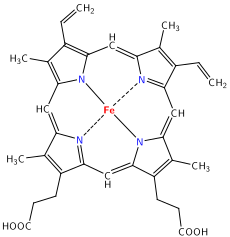
Muitos compostos orgânicos de coordenação ocorrem na natureza. Por exemplo, a hemoglobina e a mioglobina contêm um centro de ferro coordenado aos átomos de nitrogênio de um anel de porfirina; o magnésio é o centro de um anel de cloro em clorofila. O campo de tais compostos inorgânicos é conhecido como química bioinorgânica. Entretanto, a metilcobalamina (uma forma de vitamina B12), com uma ligação cobalto-metil, é um verdadeiro complexo organometálico, um dos poucos conhecidos na biologia.
Estrutura e propriedades
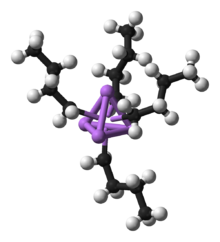
A ligação metal-carbono em compostos organometálicos está a meio caminho entre ser iônico e covalente. Os compostos organometálicos com ligações que têm caracteres entre iônico e covalente são muito importantes na indústria. Ambos são relativamente estáveis em soluções, mas iônicos o suficiente para sofrer reações. Duas classes importantes são os reagentes organolítico e Grignard.