Exemplos de nucleófilos são ânions como o Cl-, ou um composto com um par único de elétrons como o NH3 (amoníaco).
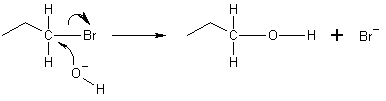
No exemplo abaixo, o oxigênio do íon hidróxido doa um par de elétrons para se ligar ao carbono no final da molécula de bromopropano. A ligação entre o carbono e o bromo sofre então uma fissão heterolítica, com o átomo de bromo tomando o elétron doado e tornando-se o íon brometo (Br-). Esta é uma reaçãoSN2 que ocorre através de ataque de retaguarda. Isto significa que o íon hidróxido ataca o átomo de carbono do outro lado, exatamente oposto ao íon bromo. Devido a este ataque de fundo, as reações SN2 resultam em uma inversão da configuração do eletrofilo. Se o eletrofilo for quiral, ele normalmente mantém sua quiralidade, embora a configuração do produto SN2 seja invertida em comparação com a do eletrofilo original (inversão Walden).
Um nucleófilo ambidente é aquele que pode atacar de dois ou mais lugares, resultando em dois ou mais produtos. Por exemplo, o íon tiocianato (SCN-) pode atacar tanto do S quanto do N. Por esta razão, a reaçãoSN2 de um halogeneto de alquilo com SCN- frequentemente leva a uma mistura de RSCN (um alquil tiocianato) e RNCS (um isotiocianato de alquilo). Misturas similares acontecerão na síntese do nitrilo de Kolbe.
Nucleófilos de carbono
Os halogenetos de metais alcalinos são nucleófilos de carbono encontrados na reação Grignard, reação Blaise, reação Reformatsky e reação Barbier, reagentes organolíticos e ânions de um alquino terminal.
As Enols também são nucleófilos de carbono. A formação de um enol é catalisada por ácido ou base. As Enols são nucleófilos ambidentes, mas, em geral, nucleófilos no átomo de carbono ao lado dos carbonos com dupla ligação (átomo de carbono alfa). As ensóis são comumente usadas em reações de condensação, incluindo a condensação de Claisen e as reações de condensação de aldol.
Nucleófilos de oxigênio
Exemplos de nucleófilos de oxigênio são água (H2O), ânion hidróxido, álcoois, ânions alcóxidos, peróxido de hidrogênio e ânions carboxilados.
Nucleófilos de enxofre
De nucleófilos de enxofre, sulfeto de hidrogênio e seus sais, os tióis (RSH), ânions de tiolato (RS-), ânions de ácidos tiolcarboxílicos (RC(O)-S-), e ânions de ditiocarbonatos (RO-C(S)-S-) e ditiocarbamatos (R2N-C(S)-S-) são os mais utilizados.
Em geral, o enxofre é muito nucleofílico devido a seu grande tamanho, o que o torna facilmente polarizável, e seus pares solitários de elétrons são facilmente acessíveis.
Nucleófilos de nitrogênio
Os nucleófilos de nitrogênio incluem amônia, azida, aminas e nitritos.
