Uma reação sigmatropica na química orgânica é uma reação pericíclica. Uma reação sigmatrópica não utiliza um catalisador e envolve uma única molécula (um processo intramolecular não catalisado). Ela transforma uma σ-bond em uma σ-bond diferente. O nome sigmatropic é o resultado de uma composição do nome há muito estabelecido "sigma" para ligações únicas de carbono carbono e a palavra grega tropos, que significa giro. Esta é uma reação de rearranjo que significa que as ligações em uma molécula mudam entre os átomos sem que nenhum átomo saia ou novos átomos sejam adicionados à molécula. Em uma reação sigmatropica, um substituto se move de uma parte de um sistema de ligação π para outra parte em uma reação intramolecular com rearranjo simultâneo do sistema π. As verdadeiras reações sigmatropicais geralmente não precisam de um catalisador. Algumas reações sigmatrópicas são catalisadas por um ácido Lewis. Reações sigmatrópicas freqüentemente têm catalisadores de metal de transição que formam intermediários em reações análogas. Os rearranjos sigmatropicos mais conhecidos são o rearranjo [3,3] Cope rearrangement, Claisen rearrangement, Carroll rearrangement e a síntese Fischer indole.
Reação sigmatropic
Visão geral dos turnos Sigmatropic
Woodward-Hoffman Sigmatropic Shift Nomenclature
Uma notação especial é usada para descrever os turnos sigmatropicais. A cada um dos átomos de carbono na espinha dorsal da molécula é atribuído um número de posição. Os rearranjos sigmatropicais são descritos por um termo de ordem [i,j]. Isto significa a migração de uma ligação σ adjacente a um ou mais sistemas π para uma nova posição (i-1) e (j-1) átomos removidos do local original da ligação σ. Quando a soma de i e j é um número par, isto é uma indicação do envolvimento de uma cadeia de átomos neutros, todos C. Um número ímpar sugere que há um átomo C carregado ou de um par heteroatômico solitário substituindo uma dupla ligação carbono-carbono. Assim, [1,5] e [3,3] turnos tornam-se [1,4] e [2,3] turnos com heteroátomos, preservando ao mesmo tempo as considerações de simetria. Os hidrogênios são omitidos no terceiro exemplo para maior clareza.

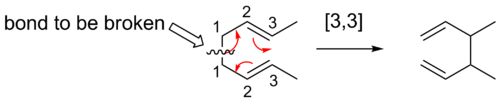
Aqui está uma maneira de encontrar a ordem de um determinado rearranjo sigmatropico. O primeiro passo é dar números a cada átomo começando com os átomos da ligação sendo quebrados como átomos 1. Os químicos contam os átomos em cada direção desde a ligação quebrada até os átomos que formam a nova ligação σ no produto. Os números que correspondem aos átomos que formam a nova ligação são então separados por uma vírgula e colocados dentro de parênteses. Isto cria o descritor de ordem de reação sigmatropic.
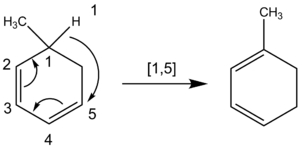
Os químicos também contam átomos ao nomear um turno sigmatropico onde um átomo de hidrogênio se move. A cadeia de carbono não se rompe em uma migração do átomo de hidrogênio. Portanto, os químicos contam em todos os átomos envolvidos na reação, em vez de apenas nos átomos mais próximos. Por exemplo, a seguinte migração do átomo de hidrogênio é da ordem [1,5], obtida pela contagem no sentido anti-horário através do sistema π, em vez da ordem [1,3] através do anel CH2 que resultaria erroneamente se contado no sentido horário.
Turnos Suprafaciais e Antarafaciais
Os químicos têm estudado reações sigmatropicais onde o grupo migrante tem um esterocentro. Em princípio, todos os turnos sigmatropicais podem ocorrer com a mesma geometria (retenção) ou o oposto (inversão) do grupo migrante. Isto depende se o lóbulo de ligação original do átomo migratório ou seu outro lóbulo é usado para formar a nova ligação.
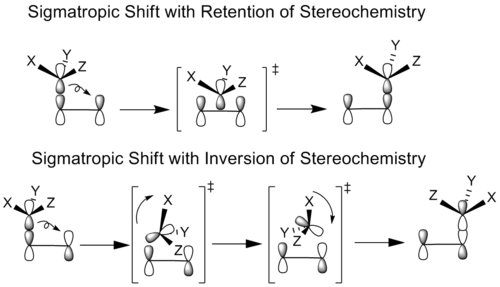
Em casos de retenção estereoquímica, o grupo migrante se traduz sem rotação para a posição de colagem. No caso de inversão estereoquímica, o grupo migrante tanto gira como se traduz para alcançar sua conformação colada.
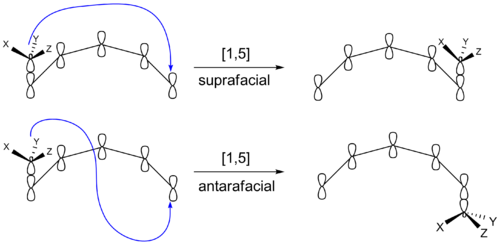
Há outra maneira que uma reação sigmatropica pode produzir produtos com esteroquímica diferente. O grupo migrante pode permanecer na face original do sistema π depois de uma nova ligação. Ou, ele pode ir para a face oposta do sistema π. Se o grupo migrante permanecer na mesma face do sistema π, o deslocamento é conhecido como suprafacial. Se o grupo migrante se transfere para a face oposta, é chamado de deslocamento antarafacial. As transformações que ocorrem dentro de anéis pequenos ou médios não podem fazer turnos antarafaciais.
Classes de Sigmatropic Rearrangements
[1,3] Turnos
Deslocamentos de hidretos térmicos
Em um turno térmico [1,3] hidreto, um hidreto move três átomos. As regras Woodward-Hoffmann ditam que ele procederia em um turno antarafacial. Embora tal mudança seja simetria permitida, a topologia Mobius exigida no estado de transição proíbe tal mudança. É geometricamente impossível. É por isso que as ferramentas não isomerizam sem um catalisador ácido ou de base.
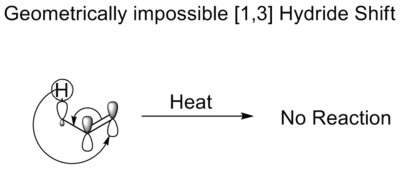
Turnos Alquílicos Térmicos
Os turnos de alquil termal [1,3], semelhantes aos [1,3] turnos de hidretos, devem proceder de forma antarafacial. A geometria do estado de transição é proibitiva. Mas um grupo alquilo, devido à natureza de suas orbitais, pode inverter sua geometria e formar uma nova ligação com o lóbulo posterior de seu sp3 orbital. Esta reação resultará em uma mudança suprafacial. Estas reações ainda não são comuns em sistemas de cadeia aberta devido à natureza altamente ordenada do estado de transição. Portanto, as reações funcionam melhor em moléculas cíclicas.
![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
Fotoquímica [1,3] Turnos
Os turnos fotoquímicos [1,3] devem ser suprafaciais; no entanto, a maioria deles não são compatíveis porque passam por um estado triplet (ou seja, têm um mecanismo dirádico, ao qual as regras Woodward-Hoffmann não se aplicam).
[1,5] Turnos
Um deslocamento [1,5] envolve o deslocamento de 1 substituto (-H, -R ou -Ar) para baixo de 5 átomos de um sistema π. Foi demonstrado que o hidrogênio se desloca tanto em sistemas de corrente cíclica quanto em sistemas de corrente aberta a temperaturas iguais ou superiores a 200 ˚C. Prevê-se que estas reações procedam de forma suprafacial, por um estado de transição de Huckel-topology.
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
A fotoirradiação exigiria uma mudança antarafacial de hidrogênio. Embora tais reações sejam raras, há exemplos em que os deslocamentos antarafaciais são favorecidos:
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)
Em contraste com os turnos de hidrogênio [1,5], nunca foram observados [1,5] turnos alky em um sistema de cadeia aberta. Os químicos têm determinado preferências de taxa para [1,5] deslocamentos alquílicos em sistemas cíclicos: carbonila e carboxila> hidreto> fenila e vinila>> alquila.
Os grupos alquílicos sofrem [1,5] turnos muito mal e geralmente requerem temperaturas elevadas. Entretanto, para as ciclohexadienes, a temperatura para os deslocamentos alquílicos não é muito mais alta do que a dos carbonilos, o melhor grupo migratório. Um estudo mostrou que isto se deve ao fato de que os deslocamentos alquílicos nas ciclohexadienes prosseguem através de um mecanismo diferente. Primeiro o anel se abre, seguido por um deslocamento [1,7], e depois o anel se reforma eletrociclicamente:
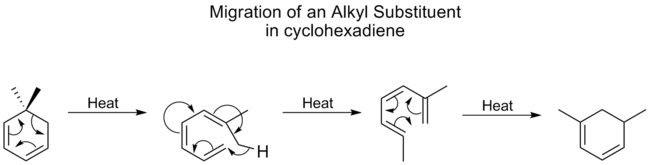
Este mesmo processo mecanicista é visto abaixo, sem a reação final de fechamento do anel eletrociclico, na interconversão do lumisterol à vitamina D2.
[1,7] Turnos
[1,7] os turnos sigmatropicais são previstos pelas regras Woodward-Hoffmann para proceder de forma antarafacial, por um estado de transição topológica Mobius. Um deslocamento antarafacial [1,7] é observado na conversão de lumisterol em vitamina D2, onde após uma abertura do anel eletrocíclico para a previtamina D2, um deslocamento de metilgênio.
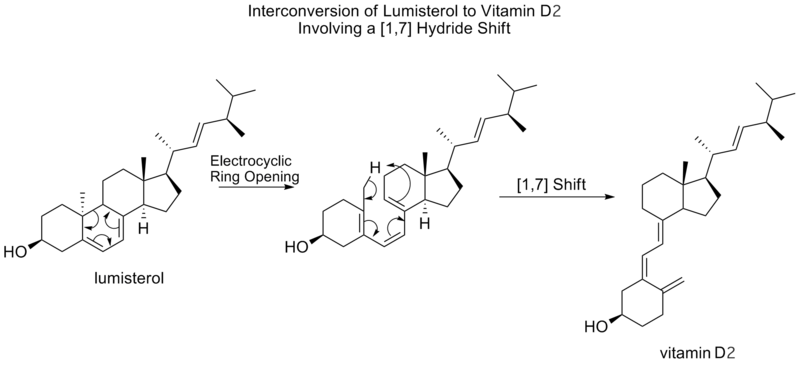
Os ciclistas nãoatrienos também passam por [1,7] turnos em um chamado rearranjo de marcha, que é o turno de um grupo divalente, como parte de um anel de três membros, em uma molécula bicíclica.
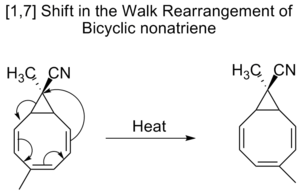
[3,3] Turnos
[3,3] os turnos sigmatropicais são rearranjos sigmatropicais bem estudados. As regras Woodward-Hoffman prevêem que estas seis reações dos elétrons procederiam suprafacialmente, usando um estado de transição da topologia de Huckel.
Rearranjo de Claisen
Descoberto em 1912 por Rainer Ludwig Claisen, o rearranjo Claisen é o primeiro exemplo registrado de um rearranjo [3,3] -sigmatropic rearranjo. Este rearranjo é uma reação útil de formação de ligações carbono-carbono. Um exemplo de rearranjo de Claisen é o rearranjo [3,3] de um éter vinílico aliado, que ao ser aquecido produz um carbonilo insaturado em γ,δ-. A formação de um grupo carbonilo torna esta reação, ao contrário de outros rearranjos sigmatropicais, inerentemente irreversível.

Rearranjo do Claisen Aromático
O rearranjo ortho-Claisen envolve o deslocamento [3,3] de um éter fenílico alélico para um intermediário que rapidamente tautomeriza para um fenol ortho-substituted.
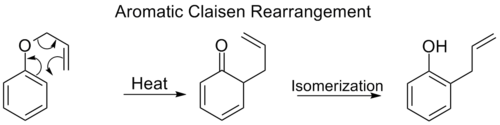
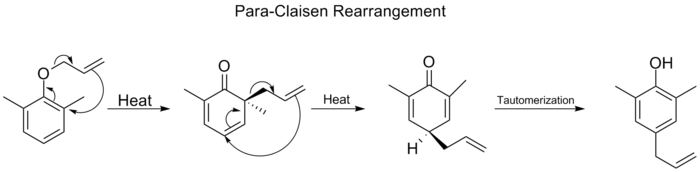
Quando ambas as posições do orto no anel de benzeno forem bloqueadas, ocorrerá um segundo rearranjo do orto-Claisen. Este rearranjo para-Claisen termina com a tautomerização a um fenol tri-substituído.
Rearranjo do cabo
O rearranjo do cabo é uma reação orgânica amplamente estudada envolvendo o rearranjo sigmatropico de 1,5-dienes [3,3]. Ela foi desenvolvida por Arthur C. Cope. Por exemplo, o 3,4-dimetil-1,5-hexadieno aquecido a 300 °C produz 2,6-octadieno.

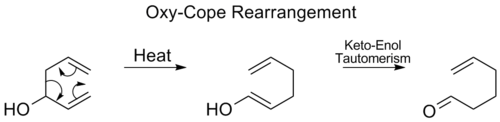
Reorganização do Oxy-Cope
O reordenamento do Oxy-Cope é adicionado um grupo hidroxil em C3 formando um enal ou enone após o tautomerismo Keto-enol do enol intermediário:
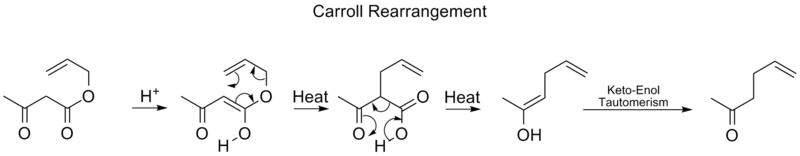
Rearranjo do rolo de papelão
O rearranjo do Carroll é uma reação de rearranjo na química orgânica e envolve a transformação de um éster alélico β-keto em um ácido α-allyl-β-ketocarboxílico. Esta reação orgânica pode ser seguida de descarboxilação e o produto final é um γ,δ-allylketone. O rearranjo de Carroll é uma adaptação do rearranjo de Claisen e efetivamente uma descarboxilação.
Síntese Fischer Indole
A síntese Fischer indole é uma reação química que produz o heterociclo aromático indole a partir de uma fenilidrazina (substituída) e de um aldeído ou cetona em condições ácidas. A reação foi descoberta em 1883 por Hermann Emil Fischer.
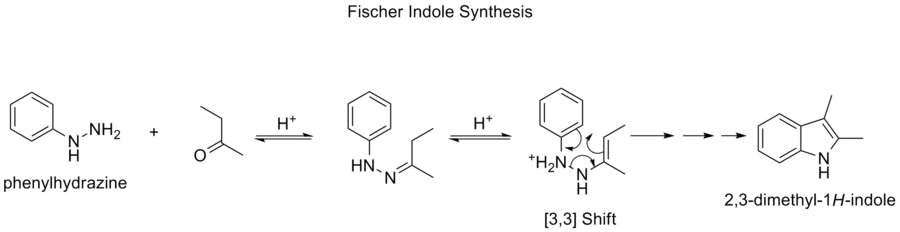
A escolha do catalisador ácido é muito importante. Os catalisadores ácidos bem-sucedidos incluem: Ácidos bronsted como HCl, H2SO4, ácido polifosfórico e ácido p-toluenossulfônico. Os ácidos Lewis, como trifluoreto de boro, cloreto de zinco, cloreto de ferro e cloreto de alumínio, também são catalisadores úteis.
Várias revisões foram publicadas.
[5,5] Turnos
Similar aos [3,3] turnos, as regras Woodward-Hoffman prevêem que [5,5] turnos sigmatropicais procederiam suprafacialmente, estado de transição da topologia Huckel. Estas reações são mais raras que [3,3] turnos sigmatropicos, mas isto é principalmente uma função do fato de que moléculas que podem sofrer [5,5] turnos são mais raras que moléculas que podem sofrer [3,3] turnos.
![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)
Rearranjos da caminhada
A migração de um grupo divalente, como O, S, NR ou CR2, que faz parte de um anel de três membros em uma molécula bicíclica, é comumente referida como um reordenamento do passeio. Isto pode ser formalmente caracterizado de acordo com as regras Woodward-Hofmann como sendo um (1, n) deslocamento sigmatropical. Um exemplo de tal rearranjo é o deslocamento de substitutos nos tropilidenos (1,3,5-cycloheptatrienes). Quando aquecido, o sistema pi passa por um anel eletrocíclico de fechamento para formar uma bicicleta[4,1,0]heptadieno (norcaradiene). Em seguida, segue um deslocamento [1,5] alquil e uma abertura do anel eletrocíclico.
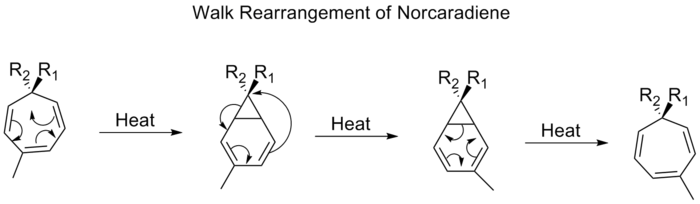
Prosseguindo por um turno [1,5], espera-se que o reordenamento da caminhada de norcaradienes proceda suprafacialmente com uma retenção de estereoquímica. Observações experimentais, entretanto, mostram que os 1,5 turnos de norcaradienes procedem de forma antarafacial. Cálculos teóricos constataram que o [1,5] turno é um processo dirádico, mas sem envolver nenhum mínimo dirádico sobre a superfície energética potencial.
Páginas relacionadas
- rearranjo 2,3-sigmatropico
- Turno NIH
- Teoria Orbital Molecular de Fronteira
- Regras Woodward-Hoffmann
Perguntas e Respostas
P: O que é uma reação sigmatrópica em química orgânica?
R: Uma reação sigmatrópica é uma reação pericíclica que envolve um processo intramolecular não catalisado e altera uma ligação σ em uma ligação σ diferente.
P: Uma reação sigmatrópica envolve um catalisador?
R: Uma reação sigmatrópica real geralmente não envolve um catalisador, embora algumas reações sigmatrópicas possam ser catalisadas por um ácido de Lewis.
P: O que significa o termo "sigmatrópico"?
R: O termo "sigmatrópico" é uma palavra composta por "sigma", que se refere a ligações simples de carbono-carbono, e a palavra grega "tropos", que significa giro.
P: Que tipo de reação é uma reação sigmatrópica?
R: Uma reação sigmatrópica é uma reação de rearranjo, o que significa que as ligações em uma molécula se deslocam entre os átomos sem que nenhum átomo saia ou novos átomos sejam adicionados à molécula.
P: O que acontece em uma reação sigmatrópica intramolecular?
R: Em uma reação sigmatrópica intramolecular, um substituinte se move de uma parte de um sistema de ligação π para outra parte com rearranjo simultâneo do sistema π.
P: Há algum rearranjo sigmatrópico bem conhecido?
R: Alguns dos rearranjos sigmatrópicos mais conhecidos são o rearranjo de [3,3] Cope, o rearranjo de Claisen, o rearranjo de Carroll e a síntese de indol de Fischer.
P: As reações sigmatrópicas geralmente envolvem catalisadores de metais de transição?
R: Sim, as reações sigmatrópicas geralmente têm catalisadores de metais de transição que formam intermediários em reações análogas.